Sistemas de nomenclatura inorgánica
El lenguaje químico debe considerarse un idioma que consta de palabras, que tiene su propia sintaxis, donde cada expresión tiene su equivalente en una fórmula química y viceversa. En este segmento aprenderás acerca de los sistemas de nomenclatura más aceptados con el objetivo de lograr un mejor entendimiento e intercambio de conocimientos con compañeros, profesores y, por qué no, también en intercambios científicos.
En el lenguaje de la química los nombres de los elementos funcionan como palabras y se unen para formar los de los compuestos, siguiendo ciertas reglas.
Para que un sistema de nomenclatura sea útil debe ser identificable, preciso y general con el fin de que se aplique a los compuestos de una función química, por lo que éstos generalmente parten de una raíz sobre la que se construye el nombre. Esta raíz puede ser el nombre de un elemento (bromo, carbono, etc.) o puede derivarse del nombre de un elemento (clor por cloro, plumb de plumbum por el plomo, ferr de ferrum por el hierro).
Además, pueden añadirse prefijos o sufijos a la raíz: hipocloroso, tricloruro, plúmbico, o bien, añadir un número, generalmente romano y entre paréntesis, por ejemplo: carbono (IV), bromo (V).
Los sistemas de nomenclatura que se revisarán son:

Aunque sin ser propiamente un sistema de nomenclatura, en éste último se señalará el nombre de algunos compuestos por uso de costumbres.
Generalidades de los sistemas de nomenclatura
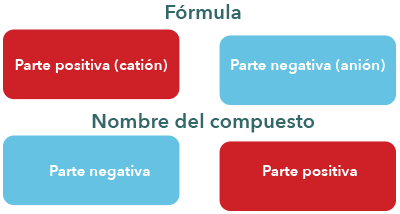
En el segmento anterior aprendiste que en una fórmula química primero se escribe el símbolo de los elementos con número de oxidación positivo y posteriormente la parte negativa. En el caso de los nombres de los compuestos la situación es contraria, es decir, primero se nombra la parte negativa y luego la positiva.
Los nombres de los ácidos en el sistema Ginebra constituyen una excepción a la regla, como se revisará más adelante.

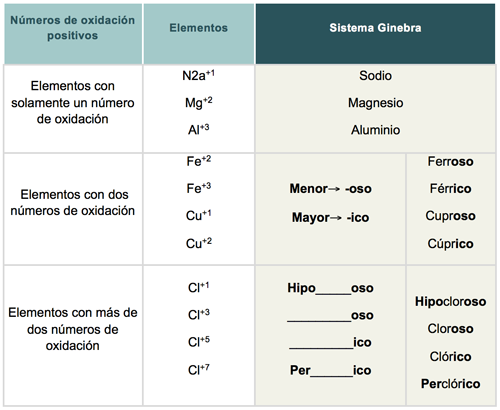
Sistema Ginebra
El nombre del compuesto resulta de la combinación de dos palabras, la primera hace referencia a la función química y la segunda al catión. Además, si el catión presenta varios estados de oxidación se utilizan prefijos y sufijos para distinguir entre éstos, de acuerdo a la regla.
Da clic sobre la imagen para ver la información
Observa el siguiente ejemplo:

Sistema Stock
En este sistema también se utilizan dos palabras para nombrarlos, la primera hace referencia a la función y la segunda al catión. Si el catión tiene varios estados de oxidación basta con colocar un número romano entre paréntesis después del nombre del catión que indique con cuál se está trabajando.
Observa el siguiente ejemplo:

Sistema de la Unión Internacional de Química Pura y Aplicada (IUPAC, por sus siglas en inglés), también conocida como nomenclatura Sistemática.
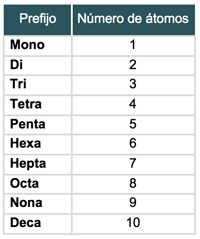
Al igual que en los dos sistemas anteriores, utiliza dos palabras: la primera es para la función y la segunda para el catión. La diferencia radica en que este sistema se basa en el uso de prefijos que indican el número de átomos de cada especie presente en el compuesto, así tenemos que:
Observa los siguientes ejemplos:

Nota: Cuando el catión cuenta con solamente un átomo no se utiliza el prefijo mono-.
Da clic en cada aparatado para conocer la información.
Hidruros metálicos

Se trata de compuestos que resultan de la unión química del hidrógeno (H1-) con un metal (M+).
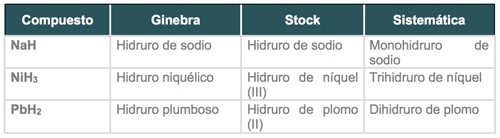
Para nombrarlos se utiliza la palabra genérica hidruro, correspondiente al hidrógeno, seguida del nombre del metal (sin dejar de considerar las reglas ya vistas para los tres sistemas).
Observa los siguientes ejemplos:
Óxidos metálicos u óxidos básicos

Resultan de la unión química del oxígeno (O2-) con un metal (M+).
Para nombrarlos se utiliza la palabra genérica óxido, correspondiente al oxígeno, seguida del nombre del metal (sin dejar de considerar las reglas ya vistas para los tres sistemas).
Observa los siguientes ejemplos:
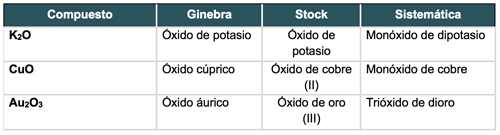
Óxidos no metálicos u óxidos ácidos

Resultan de la unión química del oxígeno (O2-) con un No metal (M+).
Para nombrarlos se utiliza la palabra óxido, correspondiente al oxígeno en los sistemas Stock y Sistemática, en el caso del sistema Ginebra se emplea la palabra anhídrido. Para mencionar el no metal se siguen las reglas ya vistas para los tres sistemas.
Observa los siguientes ejemplos:
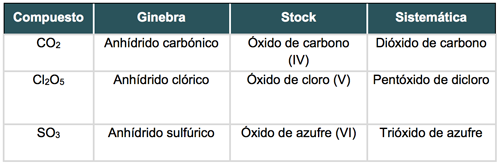
Hidróxidos o bases

Resultan de la unión química del radical hidróxido (OH1-) con un metal (M+).
Para nombrarlos se utiliza la palabra genérica hidróxido, correspondiente al radical hidróxido, seguida del nombre del metal (sin dejar de considerar las reglas ya vistas para los tres sistemas).
Observa los siguientes ejemplos:
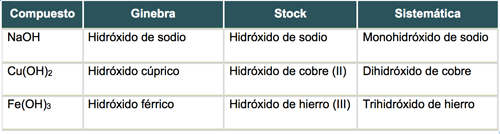
Ácidos

Se conocen con este nombre los compuestos que presentan el grupo funcional H1+ y pueden ser de dos tipos: los que contienen oxígeno en su estructura, llamados oxiácidos, y los que no contienen oxígeno: los hidrácidos.
Hidrácidos

Estos compuestos, además del hidrógeno, contienen un no metal de los grupos VIA o VIIA. En el sistema Ginebra o tradicional* (se utiliza en la disolución acuosa del compuesto) se escribe la palabra ácido, correspondiente al H1+, y el nombre del no metal con terminación hídrico.
En el sistema Stock (se usa en la fase gaseosa del compuesto) se escribe el nombre del no metal con terminación uro y después las palabras: “de hidrógeno”.
Nota: En este sistema primero se escribe la parte positiva (ácido = H1+) y luego la negativa que pertenece al no metal.
Observa los siguientes ejemplos:
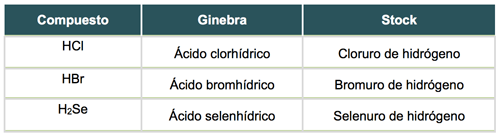
Oxiácidos u oxácidos

Estos compuestos se forman cuando reacciona un óxido ácido o anhídrido con agua, por lo tanto, los elementos que los constituyen son: hidrógeno, no metal y oxígeno.
En el sistema Ginebra se les nombra igual que en los anhídridos, solamente se cambia la palabra anhídrido por ácido.
En el sistema Stock se escribe el nombre del no metal con terminación -ato y entre paréntesis con número romano su estado de oxidación, seguido de las palabras: “de hidrógeno”.
En la nomenclatura Sistemática se indica el número de átomos de oxígeno con el prefijo correspondiente, seguido de la partícula -oxo-, unida al no metal con terminación -ato y las palabras: “de hidrógeno”.
Observa los siguientes ejemplos:
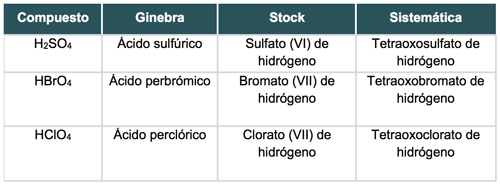
Sales

Son compuestos que resultan de la sustitución parcial o total de los hidrógenos en un ácido por metales, lo que da como resultado sales simples o haloideas, oxisales y sales ácidas.
Sales simples o haloideas

Resultan de la reacción entre un hidrácido con un hidróxido; el ión positivo es el metal y el anión el no metal. Para nombrarlos se utiliza el nombre del no metal con terminación -uro, seguido del nombre del metal (sin dejar de considerar las reglas ya vistas para los tres sistemas de nomenclatura).
Observa los siguientes ejemplos:
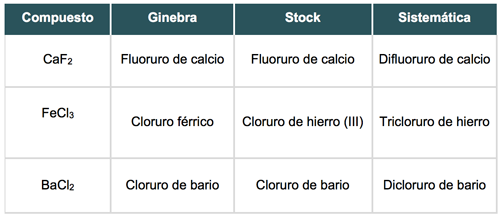
Oxisales

Resultan de la sustitución total de los hidrógenos de un oxiácido por un metal cuando reacciona con una base.
En el sistema Ginebra primero se nombra el no metal con la terminación que esté de acuerdo con el estado de oxidación, sólo se cambia la terminación -ico por -ato y la terminación -oso por -ito, seguida del nombre del metal con el sufijo que corresponde al estado de oxidación.
En el sistema Stock la primera parte del nombre es similar al sistema Ginebra, luego se nombra el metal y se indica entre paréntesis el número romano que indica su estado de oxidación.
En la nomenclatura Sistemática para nombrar el anión se indica el número de átomos de oxígeno con el prefijo correspondiente, a continuación la partícula -oxo-, unida al no metal con terminación -ato, entre paréntesis con número romano el estado de oxidación del elemento no metálico, seguido del nombre del metal, y con un prefijo se indica el número de átomos.
En el caso de que el anión se encuentre más de una vez en la fórmula se señala con un prefijo, como se indica a continuación:
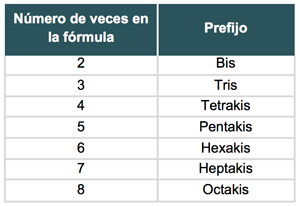
Observa los siguientes ejemplos:
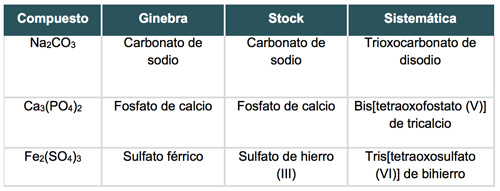
Sales ácidas

Resultan de la sustitución parcial de los hidrógenos de un oxiácido por un metal cuando reaccionan con una base.
En el sistema Ginebra se coloca la palabra ácido entre el nombre del anión y el nombre del metal, con la terminación que le compete de acuerdo con su estado de oxidación.
En el sistema Stock se nombran de manera similar a la oxisal, pero anteponiendo el prefijo hidrogen- al nombre del anión.
En la nomenclatura Sistemática se nombran de manera similar a la oxisal y también se antepone el prefijo hidrogen- al nombre del anión.
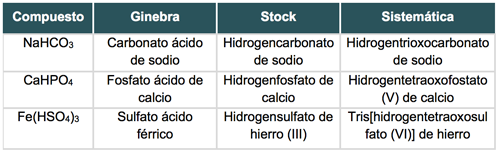
Observa los siguientes ejemplos:
Nomenclatura trivial

Este tipo de nomenclatura no sigue ningún sistema para nombrar los compuestos sino que está basada en algunas de sus características físicas, químicas, organolépticas o aplicativas. Es importante mencionar que algunos compuestos, por uso de costumbres, prefieren utilizar este nombre, aún en el ambiente científico, tal es el caso del agua (H2O, óxido de dihidrógeno) o la sal común (NaCl, cloruro de sodio).
A continuación se hace mención de algunos otros:

Como puedes observar, el nombre de estos compuestos no se relaciona con su composición química, además si existen alrededor de 100 000 compuestos inorgánicos tendrías que memorizar igual número de nombres. Se destaca la utilidad de conocer los sistemas de nomenclatura ya que, aplicando algunas reglas, puedes nombrar un gran número de compuestos.